东北制药获得药物临床试验批件
11月15日讯
东北制药(000597)11月15日晚公告,近日,公司及下属子公司东北制药集团沈阳第一制药有限公司收到国家食品药品监督管理总局核准签发的左乙拉西坦注射液及左乙拉西坦片的《药物临床试验批件》。
据了解,左乙拉西坦是比利时UCB公司研发的一种新型抗癫痫药物,于1999年经FDA批准在美国上市,主要用于治疗局限性及继发性全身癫痫,是目前美国癫痫治疗中应用最多的新型抗癫痫药物。目前左乙拉西坦原料药及片剂已在国内批准上市,UCB开发的片剂和口服溶液均已获得进口注册证,尚未见注射剂获批上市。
东北制药介绍说,根据临床试验批件显示,左乙拉西坦片注册分类为原化学药品第6类,按照《药品注册管理办法》的规定,需要进行生物等效性试验。左乙拉西坦注射液注册分类为原化学药品第3.1类,按照《药品注册管理办法》的规定,需要进行人体药代动力学试验和临床试验。公司在取得上述临床批件后,将积极进行筹备,开展临床研究。临床试验完成后,申报生产,经审批获得《药品注册批件》并有对应的获得药品GMP认证的生产线方可生产上市。
另外,东北制药还提示风险说,由于药物研发的特殊性,药物从临床试验到报批生产会受到技术、审批、政策、研究周期长等多方面因素的影响,临床试验进度及结果、未来产品生产、竞争形势均存在诸多不确定性。
[责任编辑:]
 氵厥 水一桥爆破视频回顾
氵厥 水一桥爆破视频回顾
 首届随州旅游形象大使选拔赛15强名单出炉
首届随州旅游形象大使选拔赛15强名单出炉
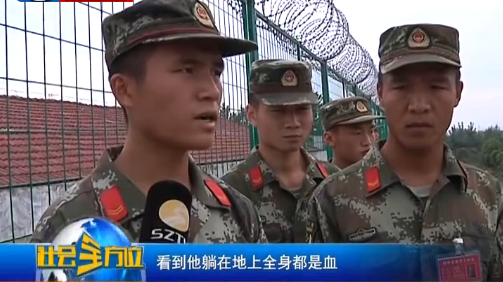 小伙夜间被捅多刀 幸遇武警战士转危为安
小伙夜间被捅多刀 幸遇武警战士转危为安
 先撞限高再撞桥 肇事司机转头跑
先撞限高再撞桥 肇事司机转头跑
 无牌摩托上街 一查竟是盗抢车
无牌摩托上街 一查竟是盗抢车
 集体财产遭破坏 村中“恶霸”谁来管?
集体财产遭破坏 村中“恶霸”谁来管?
 随州市第二届运动会青少年组跆拳道比赛举行
随州市第二届运动会青少年组跆拳道比赛举行
 随州市城投公司改善市民居住环境
随州市城投公司改善市民居住环境
 随州市举行“法律服务走近残疾人”活动
随州市举行“法律服务走近残疾人”活动
 随州高考考生走出考场
随州高考考生走出考场
 师生精心培育太空蔬菜品种
师生精心培育太空蔬菜品种











